-
Evidenziare
461432-26-8 mediatori farmaceutici
,Mediatori farmaceutici C21H25ClO6
,Mediatori farmaceutici di Dapagliflozin
-
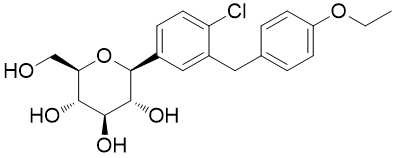
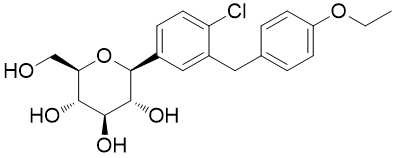
Nome di prodottoDapagliflozin
-
SinonimiDAPAGLIFLOZIN; (1S) - [(4-ethoxyphenyl) metile] fenile 1,5-Anhydro-1-C- [4-chloro-3-] - D-glucitolo;
-
CAS461432-26-8
-
MFC21H25ClO6
-
Mw408,88
-
EINECS639-683-0
-
Punto di ebollizione°C 609.0±55.0 (preveduto)
-
Densità1,349
-
Purezza99%
-
Luogo di origineLa Cina
-
MarcaRUN
-
CertificazioneIOS9001
-
Numero di modelloRUN-Z
-
Quantità di ordine minimo10g
-
Prezzoinquiry
-
Imballaggi particolari10g 50g 100g 500g 1kg
-
Tempi di consegna3-7 giorni
-
Termini di pagamentoT/T, MoneyGram, BTCcoin
-
Capacità di alimentazione1kg --100kg
461432-26-8 Dapagliflozin S1548 Selleck C21H25ClO6 639-683-0
PARTE 1: Informazioni di base
| Informazioni di base di Dapagliflozin |
| Interazioni della droga farmacologiche di sicurezza di metodo di sintesi di farmacocinesi di effetti delle droghe del diabete |
| Nome di prodotto: | Dapagliflozin |
| Sinonimi: | DAPAGLIFLOZIN; (1S) - [(4-ethoxyphenyl) metile] fenile 1,5-Anhydro-1-C- [4-chloro-3-] - D-glucitolo; Propanodiolo di Dapagliflozin; BMS-512148-05; Dapagliflozin S1548 Selleck; BASE DI DAPAGLIFLOZIN; Daglican; Dapagliflozi |
| CAS: | 461432-26-8 |
| MF: | C21H25ClO6 |
| Mw: | 408,88 |
| EINECS: | 639-683-0 |
| Categorie di prodotto: | Inibitori; Altri api; Api; Piante aromatiche; Heterocycles; Mediatori & prodotti chimici fini; Prodotti farmaceutici |
| Mol File: | 461432-26-8.mol |
| Proprietà chimiche di Dapagliflozin |
| Punto di ebollizione | °C 609.0±55.0 (preveduto) |
| densità | 1,349 |
| pka | 13.23±0.70 (preveduto) |
| Informazioni di sicurezza |
| Uso e sintesi di Dapagliflozin |
| Droghe del diabete | Dapagliflozin (ForxigaTM) è una nuova droga antidiabetica sviluppata insieme da Bristol-Myers Squibb e da AstraZeneca, essendo approvando dall'Agenzia europea per i medicinali (AME) il 12 novembre 2012. È inoltre il primo inibitore approvato SGLT2 per il trattamento del diabete di tipo II, essendo un'opzione importante nel trattamento del diabete ed è usato per migliorare il controllo glycemic come aggiunta a dietetico e l'esercizio per gli adulti con il diabete di tipo II. Dapagliflozin è un inibitore del co-trasportatore 2 del sodio-glucosio. L'8 gennaio 2014, gli Stati Uniti Food and Drug Administration (FDA) lo hanno approvato per essere utilizzato nel trattamento del diabete di tipo II. Nel frattempo, FDA richiede ai produttori di condurre la ricerca di post-marketing sui rischi relazionati con la droga. La prova di post-marketing richiesta da FDA comprende una prova cardiovascolare di risultato per la valutazione del rischio cardiovascolare per i pazienti ad alto rischio dopo il trattamento con dapagliflozin alla linea di base e ad uno studio per valutare il rischio di cancro alla vescica in pazienti reclutati. Un altro studio valuterà l'effetto dipromozione della vescica di questa droga sugli animali del roditore. Due studi valuteranno le farmacocinesi, l'efficacia e la sicurezza di dapagliflozin in pazienti pediatrici; un insieme del programma rinforzato di farmacovigilanza controllerà le anomalie del fegato ed i rapporti di risultato di gravidanza in pazienti che ricevono il daglitazone. Dapagliflozin sarà commercializzato sotto la marca Farxiga dalla farmacia di Haoeyou. Le informazioni di cui sopra sono pubblicate da Andy di chemicalbook. |
| Effetti farmacologici | Dapagliflozin funziona attraverso il trasportatore d'inibizione 2 (SGLT2), una proteina del sodio-glucosio nel rene che riassorbe il glucosio nella circolazione sanguigna. Ciò permette che il glucosio extra sia espulso attraverso l'urina, migliorante il controllo glycemic senza secrezione aumentante dell'insulina. L'uso di questa droga richiede i pazienti con la funzione renale normale mentre i pazienti di moderato ad insufficienza renale severa dovrebbero essere disabili usare questa droga. La singola applicazione di questo prodotto o combinazione con metformina, il pioglitazone, il glimeperide, l'insulina ed altre droghe può ridurre significativamente il HbA1c e la glicemia a digiuno dei pazienti che soffrono il diabete di tipo II. La frequenza della reazione avversa era simile a placebo con a basso rischio dell'ipoglicemia, potendo ridurre il peso corporeo. L'efficacia di dapagliflozin è comparabile con gli inibitori della peptidasi di dipeptidil e parecchi nuovi ipoglicemizzanti e può anche abbassare leggermente la pressione sanguigna ed il peso corporeo. La droga ha 5mg e le compresse 10mg due da scegliere da, possono essere utilizzate da solo o insieme ad insulina, compreso altre droghe del diabete. |
| Farmacocinesi | Negli individui sani, il dapagliflozin rapidamente è stato assorbito dopo la somministrazione orale con un tempo di punta Tmax che è di 1 - 2 ore, un tasso del grippaggio della proteina di 91%, una biodisponibilità orale di circa 78% e un'emivita terminale del plasma di 12,9 ore. Dopo la somministrazione orale, la droga pricipalmente è metabolizzata dal glucuronosyltransferase difosfato 1A9 (UGT1A9) dell'uridina nel metabolita inattivo nel fegato con la più piccola parte che è metabolizzata dall'enzima P450 e di nessun effetto inibitorio o d'induzione sull'enzima P450. I prototipi della droga ed i metaboliti relativi sono stati espelsi attraverso urina (75%) e feci (21%). Paragoni l'amministrazione simultanea di questo prodotto ad alimento ad alta percentuale di grassi e con l'amministrazione di digiuno, Tmax può essere esteso da 1 volta, ma l'assorbimento non ha colpito il grado, in modo da può essere amministrato insieme all'alimento. Le farmacocinesi del daglitazone sono state colpite significativamente dalla funzione renale. I pazienti diabetici con insufficienza renale delicata, moderata o severa sono fusi per essere conforme ad una somministrazione orale di 20 mg • daglitazone d-1 per 7 giorni. L'importo sistemico medio dell'esposizione, rispetto ai pazienti con la funzione renale normale, è rispettivamente 32%, 60% e 87% più alti. Per i pazienti con la funzione renale normale, l'insufficienza delicata, l'insufficienza moderata e l'insufficienza severa, la quantità urinaria dell'escrezione del glucosio in 24 ore dello stato di stabilità era 85, 52, 18 e 11g, successivamente. Kasichayanula ed altri hanno studiato gli effetti farmacocinetici di disfunzione del fegato sul daglitazone. I pazienti con insufficienza epatica delicata, moderata e severa che ha una singola dose orale di 10 mg di daglitazone, il Cmax di ogni gruppo erano 12% si abbassano, 12% più alti e 40% superiori a quello con la funzione epatica normale, rispettivamente. Il AUC di ogni gruppo era significativamente superiore a quello della funzione epatica normale da 3%, da 36% e da 67%. Di conseguenza, non è raccomandato per applicare il daglitazone ai pazienti di disfunzione renale moderata e severa. I pazienti severi di disfunzione del fegato devono ridurre l'uso della dose. |
| Metodo di sintesi | l'acido 5-bromo-2-chlorobenzoic è conforme a clorazione acylating ed ha reazione dei Friedel-mestieri con etere feniletilico per riduzione del suo gruppo carbonilico, generante un metano di 5 bromo-2-chloro-4'-ethoxydiphenyl, più ulteriormente sottoponente alla condensazione con 2, 3, 4, 6 acid-1,5-lactone tetra-O-trimetilsililici-D-GLUCOPYRANOSANOIc. Il gruppo di idrossile anomerico del carbonio è conforme all'eterificazione e al deprotection per dare 2 chloro-5- (1-methoxy-D-glucopyranose-I-yl) - 4' - ethoxydiphenylmethane e poi usare Et3SiH/BF3 • OEt2 affinchè riduzione rimuovano metossilico, seguito da esterificazione e da idrolisi acetiche dell'anidride per dare ad agenti ipoglicemici daglitazone con il rendimento globale di circa 40%. Fig.1 mostra l'itinerario della reazione chimica della sintetizzazione del dapagliflozin. |
| Sicurezza | Daglitazone ha la tolleranza e sicurezza eccellenti con l'incidenza degli eventi avversi connessi con 10 mg • daglitazone d-1 che è simile a quello di placebo. Gli eventi avversi comuni hanno compreso l'ipoglicemia, la poliuria, il dolore alla schiena, l'aumento genitale di infezioni, di infezioni delle vie urinarie, di dislipidemia e dell'ematocrito (HCT). Il rischio globale di ipoglicemia è basso e l'incidenza dell'ipoglicemia è associata con altri agenti ipoglicemici di base. L'incidenza dell'ipoglicemia era più alta in pazienti che sottopongono per congiungere il trattamento fra il daglitazone e sulfoniluree o insulina rispetto a placebo. Di conseguenza, quando questo prodotto è usato congiuntamente ad insulina o al secretagogue dell'insulina, potete avere bisogno di di regolare la dose di quella posteriore. |
| Interazioni della droga | Questo prodotto pricipalmente è metabolizzato nel fegato da metabolismo UGT1A9, essendo il substrato della glicoproteina P. Lo studio ha confermato che le farmacocinesi del daglitazone non sono state colpite da metformina, pioglitazone, sitagliptina, glimeperide, voglibose e simvastatine, valsartan, warfarin e digossina. Le concentrazioni nel siero delle droghe suddette non sono clinicamente inoltre significativamente colpite dal daglitazone. La rifampicina può ridurre la quantità dell'esposizione di daglitazone di 22% mentre l'acido mefenamic può aumentare l'importo dell'esposizione del corpo di 51%, ma ha non non clinicamente effetto significativo su 24 escrezioni del glucosio dell'urina di h. |
| Descrizione | L'amministrazione terapeutica australiana delle merci (TGA) e la Commissione Europea hanno approvato il dapagliflozin a ottobre e novembre 2012, rispettivamente, come aggiunta per essere a dieta ed esercitarsi per il trattamento del diabete di tipo 2. Dapagliflozin è una terapia potenzialmente attraente dovuto il suo meccanismo dell'insulina-indipendente e glucosesensitive di azione. È SGLT2 un inibitore selettivo classe prima (IC50=1.1nanometro; selettivitàcontroSGLT1>1000)cheabbassalasogliarenaleperriassorbimentodiglucosio, permettendo cheilglucosioin eccessosi eliminiviaireni. Inrattinormali, l'amministrazionedidapagliflozinpromuovel'escrezionedipendente dalla dosedimgfino a1900diglucosiosui24periodidih, coneffettoamaximala3mg/kg. In unratmodeldidiabete, pretrattamentoconirisultatipancreaticidistreptozotocindellatossinanell'iperglicemiacheè ridotta55%tramitel'amministrazionedisingoladosedi0,1mg/kgdidapagliflozinrispettoalveicolo. Gliinibitoriarilicidel O-glucosideSGLT2eranodebuttantiin anticiponellaclinica, maillegamearilicodel C-glucosidetrovatoneldapagliflozinconferiscelaresistenzaametabolismoglucosidasi-mediatocheconduceall'utilitàclinicamiglioreriguardantei O-glucosidiarilici. Illegamemodificatodell'carboidrato-agliconeha richiestol'adeguamentoconcomitanteda unortoad unarylglucosidemeta-sostituitodi raggiungerel'inibizionepotenteSGLT2. Dapagliflozinè stato sintetizzatoaparecchipuntivialareazionedi unaryllithiumcongluconolattoneper-sililatoper formareillegamechiavedel C-glucoside. Unariduzionealfa-selettivadelglicosideanomericorisultanteha datoilbeta-Carylglucosidedesiderato. Ilmetabolita(inattivo)dicircolazioneprincipaleèilrisultatodi3-O-glucuronidationdelglucosylmoiety. Deimetabolitidiminoranza, lespecieossidativeprincipaliderivanodalla O-dealchilazionedel ethoxy-gruppoedell'idrossilazionedellapartedelbiarylmethane. |
| Proprietà chimiche | Solido bianco |
| Creatore | Bristol-Myers Squibb (Stati Uniti) |
| Usi | Un inibitore del trasportatore 2 del sodio-glucosio. |
| Usi | terapeutico per diabete io o II e l'iperglicemia |
| Definizione | ChEBI: Corrente alternata - beta-D-glucosio comprendente glicosilico in cui il gruppo idrossilato anomerico è sostituito da un gruppo fenile di 4 chloro-3- (4-ethoxybenzyl). Usato (nel formo f il suo monoidrato del propanodiolo) per migliorare ontrol glycemic, con la dieta e l'esercizio, in adulti con il diabete di tipo 2. |
| Marca commerciale | Forxiga |